1 . Hémoglobinopathies .
Il existe différentes formes d'hémoglobines ; Hb A , Hb A2, Hb fœtal.
a) Définition.
L'hémoglobinopathie est toute maladie où les acides aminés de la séquence primaire de l'hémoglobine sont atteints (chaîne alpha ou béta).
Au niveau du poumon, 95% de l'Hb est sous forme d'oxyHb.
Au niveau du muscle, la PP étant < à 20 mmHg, moins de 20% de l'Hb est sous forme d'oxyHb.
L'hémoglobine peut aussi fixer le CO2 et les H+. C'est l'histidine (146 beta et 120 alpha) qui fixe les H+ ce qui modifie l'affinité de l'Hb pour l'O2.
L'hémoglobinopathie peut être due à ;
- Une délétion d'acides aminés.
- Une insertion (addition) d'un acide aminé.
- Une substitution d'un acide aminé par un autre.
Ce qui entraîne une modification de la structure primaire de l'Hb et donc une modification de son affinité pour l'O2. Les hémoglobinopathies sont bien connues chez l'homme, moins bien chez les animaux.
b) technique.
L'électrophorèse est la technique utilisée pour ces études. Si un acide aminé avec une charge- est remplacé par un autre avec une charge+, au sens large, la mobilité sera différente.
c) exemples.
- Anémie falciforme.
Les GR sont en faucille : l'Hb S ce qui modifie léffinité de l'hB pour l'O2.

- Hémoglobines instables : corps de Heinz.
Dans ce cas, l'HB à une solubilité réduite et est instable. Cela provient d'une substitution d'acides aminés dans la zone proche de l'hème qui provoque une déformation de l'Hb avec apparition de groupes –SH de cystéine en surface. L'Hb va alors réagir avec une autre molécule d'Hb et créer des ponts di sulfures ce qui provoque leur précipitation. C'est ce que l'on appelle un corps de Heinz.
- Signes cliniques : anémie, ictère, splénomégalie, diminution de l'hématocrite, diminution de la concentration en Hb.
- Diagnostic : - test de stabilité à la chaleur
- test de précipitation à l'isopropanol. L'Hb ne précipite pas, l'Hb anormale précipite.
- Hémoglobine ayant une affinité anormale pour l'O2.
En général, l'affinité augmente, c-à-d que l'Hb a plus difficile à libérer l'O2.
Signes cliniques : hypoxie, stimulation de la synthèse des GR, polycytémie (augmentation du nombre des cellules sanguines).
- Méthémoglobine (HbM).
Il y a du Fe+++ (ferrique) à la place du Fe++ (ferreux. Il y a par conséquent impossibilité de fixer l'O2. Cela se produit lors de déficience en méthémoglobine réductase chez le chien. Cet enzyme est normalement présent dans le GR.
Diagnostic : modification du spectre d'absorption.
2. Thalassémies .
Maladie existant au pourtour de la Méditérrannée mais qui ne concerne pas les animaux. C'est une insuffisance de production de ;
- soit de la globine alpha (thalassémie alpha)
- soit de la globine bêta (thalassémie bêta)
provenant d'une déficience de gênes codant pour alpha et bêta.
1. Déficiences enzymatiques .
a) métabolisme des érythrocytes .
Le globule rouge n'a ni noyau, ni microsomes (donc pas de synthèses) ni de mitochondries (donc pas de respiration, c-à-d pas de phosphorylations oxydatives).
MAIS l'oxygène diffuse quand même dans le globule rouge (Hb fixe 95% et les 5% qui ne sont pas fixés par l'Hb provoquent des dégâts : il faut des oxydations.
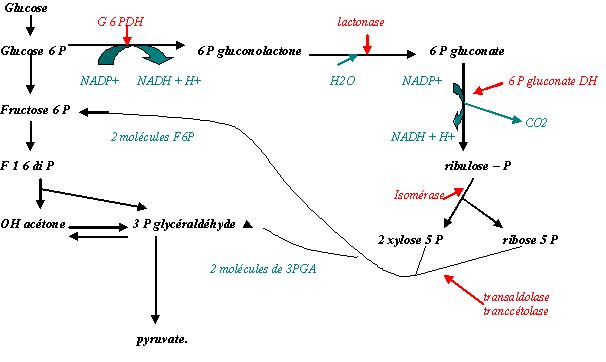
L'utilisation du glucose se fait par la glycolyse et par la voie des pentoses phosphates (shunt des pentoses).
a) la glycolyse.
Au cours de la glycolyse, du NAD+ est transformé en NADH + H+.
Mais pour continuer la glycolyse, il faut régénérer le NAD+. Cela se fait de 3 façons :
La majorité du glucose est transformée par la glycolyse dans le GR :
- 60 % est transformé en lactate
- 30% en 2-3DPG
- 5 à 10 % passe dans la voie des pentoses phosphate.
Le rôle de la glycolyse est de fabriquer de l'ATP qui est utilisé par l'ATPase de la pompe Na+/K+ qui est normalement présente dans le GR.
En général, le K+ intracellulaire est élevé (sauf chez le chien et le chat), il y a très peu de K+ intracellulaire (seulement 2 fois plus que le K+ sanguin. Ceci est du à une absence d'ATPase (en fait il a beaucoup moins car l'ATPase existe dans tous les GR).
- Chez le chien et le chat, l'activité ATPasique est faible.
- Chez le cheval, le bovin et certains moutons, l'activité ATPasique est très faible.
- Chez le porc, l'homme et certains moutons, l'activité ATPasique est très forte.
Utilité du 2-3 di phosphoglycérate (2-3 DPG).
Il se lie à la désoxyhémoglobine et diminue son affinité pour l'O2 ( P50>>> PH, PCO2 )
Donc une fois que l'Hb a libéré son O2, elle se fixe à la 2-3 DPG.
En cas d'hypoxie, il y a peu d'oxyHb et donc beaucoup de désoxyHb et donc beaucoup de 2-3DPG se fixe à la désoxyHb . En conséquence, il faut augmenter la synthèse de 2-3DPG par la mutase.
Comme il y a moins de 2-3 di phosphoglycétrate libre, il n'y a plus de rétro inhibition de la mutase par le 2-3DPG et donc l'enzyme synthétise des quantités accrues de 2-3 DPG. Ce phénomène se produit notamment en montagne où l'oxygène diminue et donc l'oxyHb diminue aussi.
Le 2-3 DPG permet de diminuer l'affinité de l'hémoglobine pour l'oxygène en basse pression d'O2 (L'Hb relargue une partie de son O2). le 2-3 DPG compense donc l'hypoxie.
- le chien, le cheval et l'homme ont beaucoup de 2-3 DPG, il ya donc une modification de l'affinité de l'Hb pour l'oxygène par le 2-3 DPG.
- le chat, le bovin, le mouton ont peu de 2-3 DPG car la mutase est peu active (ct). Chez ces espèces, si on enlève le 2-3 DPG sérique, il n'y a pas d'augmentation de l'affinité de l'Hb pour l'oxygène. Si on ajoute du 2-3 DPG, il n'y a pas de diminution de l'affinité de l'Hb pour l'oxygène. Il n'y a donc pas de corrélation entre le 2-3 DPG et l'affinité de l'Hb pour l'oxygène. Chez ces espèces, en cas d'hypoxie, il n'y a pas de compensation par le 2-3 DPG, l'hypoxie est par conséquent accrue.
b) Voie des pentoses phosphates .
Rôle du NADPH.
Il permet le maintien - de l'hémoglobine sous forme non oxydée
- du glutathion sous forme réduite.
Or, on vu que l'O2 libre (5%) au niveau du GR provoque ;

Le FMN est le coenzyme de nombreuses déshydrogénases intervenant dans des réactions d'oxydo-réduction. Le glutathion réductase possède une FMN sans lequel il ne peut pas agir.
Donc toute carence en Vit B2 provoque une oxydation de l'Hb et de l'anémie hémolytique.
1) Déficience en sélénium .
La glutathion peroxydase possède 4 molécules de sélénium. S'il y a carence alimentaire en sélénium, il y a anémie hémolytique.
2) Déficience en G6P déshydrogénase ( G6PDH) .
Normalement tout vieux GR est détruit par la rate. Lorsqu'il n'y a plus de G6PDH, il n'y a plus de correction de l'Hb oxydée. En conséquence, l'Hb peut réagir avec le groupe –SH des protéines et précipiter sous forme des corps de Heinz. Les corps de Heinz entraînent une déformation du GR qui est reconnue par la rate. Celle-ci détruit alors le GR.
1. Déficiences membranaires .
Coupe de la membrane du globule rouge.
Elle est constituée de 35 à 45 % de lipides, le reste est constitué de carbohydrates.
a) la membrane intervient-elle dans la survie des globules rouges ?
La survie normale d'un globule rouge est de 120 à 160 jours. En fait cela varie d'une espèce à l'autre. cela survient surtout en cas d'atteinte enzymatique (au niveau du NADPH) qui provoque une diminution de survie des globules rouges par déformation de la membrane.
Survie des GR chez le chien ; 86 à 106 jours et chez le chat ; 65 à 70 jours
b) anomalies .
- Sphérocytose .
La cellule est anormalement perméable au Na+ qui entre massivement et provoque un gonflement du GR. La rate les reconnaît comme anormaux et les détruit. Il y donc suite à cela une anémie hémolytique et une splénomégalie. Cela se produit chez le chien lors de maladie hémolytique auto immune.
Comme il y a anémie, il y a augmentation du nombre de réticulocytes et donc MCV (taille) diminue et MCHC (teneur en Hb) augmente.
Chez l'homme, il existe aussi une déficience héréditaire en G6PDH.
- Corps de Heinz.
Les globules rouges forment entre eux des ponts disulfures suite à une anomalie de la membrane. Ces GR sont détruits par la rate. Cela se produit ;
- dans tous les cas où il y a une déficience de G6PDH. (qui produit le NADPH par le shunt des pentoses phosphates).
- chez le chat lorsque l'on administre du bleu de méthylène.
- Chez le cheval après traitement à la phénothiazine.
- Chez les herbivores qui pâturent dans des prairies où il y a des oignons sauvages.
L'animal le plus sensible est le chat car il possède beaucoup plus de cystéine (-SH) que les autres espèces. ( 8 groupes –SH libres).
L'animal le moins sensible est le mouton.